前列腺癌(Prostate cancer, PCa)是威脅中老年男性健康的主因之一。在2024年全球男性腫瘤發病率和死亡率統計中,PCa分别排第二和第五位[1]。雄激素和雄激素受體(Androgen receptor,AR)在PCa的發生發展中起核心作用,故臨床上對早期PCa患者主要采取抗雄治療(Androgen deprivation therapy,ADT)。ADT對原位癌(primary PCa)療效顯著,但對晚期或複發性癌症的療效有限;而且腫瘤對ADT的耐藥性不可避免,幾乎所有的病人都會在1-2年内以去勢抵抗性前列腺癌(Castration-resistant PCa,CRPC)的形式複發。目前,CRPC在世界範圍内基本是不治之症,是晚期PCa患者死亡的主因,其根本原因在于分子機制尚不明确,且對現有的免疫治療方案不敏感,導緻缺乏有效的治療靶點和策略[2]。
蛋白質精氨酸甲基化是哺乳動物中最常見的翻譯後修飾之一,也是近年來備受關注的癌症研究熱點;該過程主要由PRMT (protein arginine methyltransferases, PRMTs) 基因家族調控。PRMTs家族共包括9個成員(PRMT1-PRMT9),組織表達譜廣泛,可以以3種不同的形式(Ⅰ、Ⅱ和Ⅲ型)對底物進行修飾。研究表明,PRMTs酶活性的改變、基因突變/缺失與癌症的發生發展或/和轉移密切相關[3]。作為最主要的Ⅱ型精氨酸甲基化修飾酶,近年盡管有少量研究發現PRMT5在PCa中異常激活,但其在惡性PCa中的确切生物學功能及潛在分子機制尚不清楚,且PRMT5和AR之間是否存在直接調控關系存在明顯争議[4]。
近日,2003网站太阳集团的張定校教授團隊聯合東南大學附屬中大醫院泌尿科許斌團隊,在Cancer Letters (IF=9.756)上在線發表了題為Inhibition of PRMT5 moderately suppresses prostate cancer growth in vivo but enhances its response to immunotherapy的原創性研究論文。該工作揭示了PRMT5通過MYC軸調控PCa惡性生物學行為的分子機制,并通過動物模型證實了靶向PRMT5聯合免疫治療是治療CRPC新的可行方案。

首先,作者利用臨床組織樣本結合公共數據庫,确認了PRMT5在腫瘤組織中的上調表達,并發現其與病人的不良預後相關。細胞生物學試驗表明,利用shRNA降低PRMT5的表達水平或利用小分子抑制劑EPZ015666(PRMT5i)特異性地抑制其酶活性後,腫瘤細胞的增殖、侵襲、幹性(stemness)等多種惡性生物學行為均受到顯著抑制;且随着細胞惡性程度的升高,其受到的影響也更加明顯。分子機制方面,作者利用不同處理條件下的RNA-seq、Cut&Tag和公共數據分析發現,PRMT5可以促進cancer-promoting相關通路(如增殖、DNA損傷修複、幹性等)進而發揮促癌功能。鑒于AR在PCa發生發展中的核心角色,作者全方位探究了PRMT5與AR之間的關系,證實兩者之間并不存在直接的調控作用。而與之相對應的,PRMT5與核心緻癌因子MYC組成強烈的正反饋調控軸。
PCa是典型的“冷”腫瘤,免疫細胞浸潤水平低,導緻病人對免疫治療應答率低。作者發現PRMT5對PCa的免疫活性起負調控作用,由此設想:能否通過抑制PRMT5活性提升腫瘤整體免疫水平,将其由“冷”變“熱”,再進行免疫治療,對腫瘤細胞進行有效殺傷?為此,作者利用NSG、RM1和TRAMP等系列小鼠模型,分别檢測PRMT5i、anti-PD-1單藥和聯合用藥對腫瘤的抑制效果。結果顯示,PRMT5i和anti-PD-1單藥處理僅能較弱地抑制體内腫瘤的生長,而雙藥連用則展現出更佳的抑癌作用(A)。最後,由于PRMT5i單藥的作用較溫和,那它是否能和其他現有的一些癌症治療藥物聯合使用,增加藥效?受合成緻死概念的啟發,作者利用全基因組CRISPR/Cas9篩選技術,挖掘了一系列潛在和PRMT5起協同效應的治療靶标(B),比如PRMT5i可以顯著增強PARPi對CRPC癌細胞的殺傷效果(值得後續進一步的預臨床和臨床研究)。
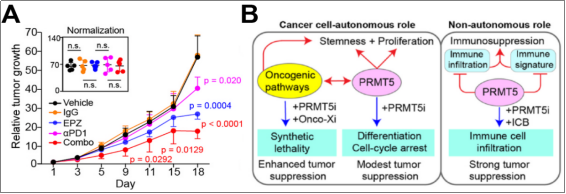
該項研究中,作者利用生信分析和細胞/分子生物學手段,全方位探究了PRMT5對腫瘤細胞的調控作用,并揭示了3種以靶向PRMT5為核心的潛在治療CRPC的方案:1)PRMT5i可通過抑制cancer-promoting相關通路對腫瘤細胞的惡性表型起一定的抑制作用;2)PRMT5i聯合免疫治療可對腫瘤産生顯著殺傷;3)PRMT5i聯合靶向其他腫瘤協同因子藥物可進一步提升抗腫瘤效果(B)。因此,作者為明晰PRMT5在PCa中的功能和分子機制提供了新的認知,為其潛在的臨床應用提供了理論和試驗基礎(已有不同公司的多款PRMT5i在進行臨床試驗)。
張定校實驗室的博士生賀琴菊、張元祯,東南大學許斌團隊李文超醫師和博士生陳賽賽為論文的共同第一作者。張定校教授、博士後鄒成和東南大學許斌教授為論文共同通訊作者。該工作受到了中南大學湘雅醫院袁凱教授的大力支持!課題組長期招收保研生和直博生,并熱忱歡迎具有生命醫學背景的博士後加盟!
全文銜接:https://www.sciencedirect.com/science/article/pii/S0304383524006098
參考文獻:
1. Siegel RL, Giaquinto AN, Jemal A: Cancer statistics, 2024. CA: a cancer journal for clinicians 2024, 74(1):12-49.
2. Zhang D, Zhao S, Li X, Kirk JS, Tang DG: Prostate Luminal Progenitor Cells in Development and Cancer. Trends in cancer 2018, 4(11):769-783.
3. 何伶靖, 鄒成, 賀琴菊, 馮宇晴, 張定校. PRMT5在癌症中的研究進展. 中國細胞生物學學報 2021, 43 (03).
4. Qinju He, Yuanzhen Zhang, Wenchao Li, Saisai Chen, Jiangling Xiong et al.: Inhibition of PRMT5 moderately suppresses prostate cancer growth in vivo but enhances its response to immunotherapy. Cancer Letters 2024, 31:602:217214.